Chào mừng bạn đến với chuyên mục kiến thức hóa học thực tiễn tại Korea House năm 2026 hôm nay. Trong bài viết này, Chef Kim sẽ hướng dẫn bạn cách xác định hno3 công thức cấu tạo một cách chi tiết. Việc nắm vững cấu trúc phân tử này giúp chúng ta hiểu rõ hơn về tính chất axit mạnh của nitric acid. Đây là kiến thức nền tảng quan trọng cho học sinh và cả những người yêu thích khoa học đời sống.
Tổng quan về phân tử nitric acid và ý nghĩa cấu trúc
Để bắt đầu tìm hiểu về hno3 công thức cấu tạo, chúng ta cần hiểu rõ về bản chất của hợp chất này. Nitric acid là một axit vô cơ mạnh, có tính oxy hóa cực kỳ cao trong các phản ứng hóa học cơ bản. Trong đời sống, hợp chất này đóng vai trò quan trọng trong việc sản xuất phân bón và các loại thuốc nổ hữu ích. Hiểu rõ cấu tạo phân tử giúp bạn giải thích được tại sao nó lại có khả năng ăn mòn kim loại mạnh.
Việc xác định chính xác hno3 công thức cấu tạo sẽ dựa trên việc phân bổ các electron hóa trị của từng nguyên tử. Mỗi liên kết trong phân tử đều tuân theo những quy luật vật lý và hóa học rất khắt khe về năng lượng. Chef Kim nhận thấy rằng việc học cấu trúc hóa học cũng giống như việc chuẩn bị nguyên liệu cho một món ăn. Nếu bạn nắm chắc thành phần nguyên tử, việc lắp ghép chúng lại thành một phân tử hoàn chỉnh sẽ rất dễ dàng.
Mẹo nhỏ từ Chef Kim: Hãy luôn ghi nhớ số electron lớp ngoài cùng của các nguyên tố phi kim chính để vẽ nhanh hơn. Nitơ luôn có 5 electron, trong khi Oxy có 6 và Hydro chỉ có duy nhất 1 electron để tham gia liên kết.
Bảng thành phần “nguyên liệu” để xây dựng phân tử HNO3
Dưới đây là bảng liệt kê các thành phần nguyên tử cần thiết để thiết lập hno3 công thức cấu tạo chính xác.
| Nguyên tử | Số lượng | Số electron hóa trị | Mục tiêu đạt bát tử (Octet) |
|---|---|---|---|
| Hydro (H) | 01 | 01 | Cần thêm 1 electron (đạt cấu hình Heli) |
| Nitơ (N) | 01 | 05 | Cần thêm 3 electron để đạt trạng thái bền |
| Oxy (O) | 03 | 06 | Mỗi nguyên tử cần thêm 2 electron để bền |
Để tạo nên hno3 công thức cấu tạo hoàn chỉnh, tổng số electron hóa trị có sẵn là 24 thành phần đơn lẻ. Con số này được tính từ: 1 (H) + 5 (N) + 6 x 3 (O) bằng đúng 24 electron hóa trị thực tế. Việc kiểm soát tổng số electron này cực kỳ quan trọng để đảm bảo bạn không vẽ thừa hoặc thiếu liên kết.
Chi tiết các bước xác định hno3 công thức cấu tạo chính xác
Bước 1: Phân tích sự hình thành cặp electron dùng chung
Trong quy trình xây dựng hno3 công thức cấu tạo, bước đầu tiên là xác định cách thức các nguyên tử chia sẻ electron. Nguyên tử Hydro sẽ bỏ ra 1 electron để góp chung với 1 electron từ nguyên tử Oxy thứ nhất trong mạch. Nguyên tử Oxy này cũng đồng thời bỏ ra thêm 1 electron khác để liên kết trực tiếp với nguyên tử Nitơ trung tâm. Điều này tạo ra một sợi dây liên kết mạch thẳng nối giữa Hydro, Oxy và Nitơ trong sơ đồ phân tử.
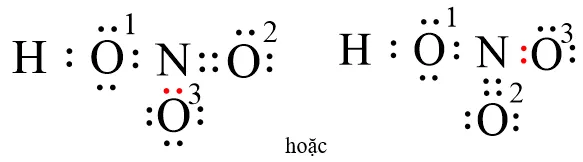 Mô phỏng sự góp chung electron trong phân tử HNO3Thông tin chi tiết về sự phân bổ các cặp electron dùng chung giữa các nguyên tử Nitơ và Oxy.
Mô phỏng sự góp chung electron trong phân tử HNO3Thông tin chi tiết về sự phân bổ các cặp electron dùng chung giữa các nguyên tử Nitơ và Oxy.
Tiếp theo, nguyên tử Nitơ và nguyên tử Oxy thứ hai sẽ cùng bỏ ra mỗi bên 2 electron hóa trị quan trọng. Hành động này tạo thành một liên kết đôi bền vững, giúp cả hai nguyên tử tiến gần hơn tới quy tắc octet. Lúc này, cả Nitơ và hai nguyên tử Oxy đầu tiên đã đạt được trạng thái bão hòa electron theo lý thuyết hóa học. Bạn sẽ thấy rõ sự phân bổ này khi bắt đầu vẽ các dấu chấm đại diện cho electron trên giấy.
Bước 2: Hình thành công thức electron thực tế
Sau khi đã xác định được các cặp dùng chung, chúng ta sẽ biểu diễn chúng dưới dạng hno3 công thức cấu tạo electron. Đối với nguyên tử Oxy thứ ba, nó vẫn chưa đạt được trạng thái bền vững với 8 electron ở lớp ngoài cùng. Trong trường hợp đặc biệt này, nguyên tử Nitơ sẽ sử dụng một cặp electron độc thân chưa liên kết của chính mình. Cặp electron này sẽ được “cho” để dùng chung với Oxy thứ ba mà Oxy không cần đóng góp thêm electron nào.
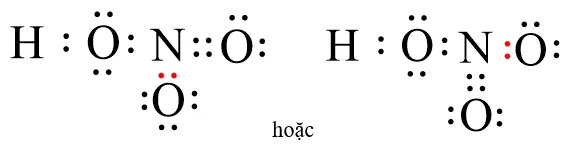 Biểu diễn công thức electron hoàn chỉnh của phân tử axit nitricCách sắp xếp các dấu chấm electron xung quanh các ký hiệu hóa học để tạo thành phân tử bền.
Biểu diễn công thức electron hoàn chỉnh của phân tử axit nitricCách sắp xếp các dấu chấm electron xung quanh các ký hiệu hóa học để tạo thành phân tử bền.
Trong bảng biểu diễn hno3 công thức cấu tạo này, Nitơ đóng vai trò là nguyên tử cho, còn Oxy là nguyên tử nhận. Kết quả là chúng ta có tổng cộng 5 cặp electron dùng chung giữa tất cả các nguyên tử trong phân tử axit này. Ngoài ra, phân tử còn sở hữu 7 cặp electron tự do thuộc về các nguyên tử Oxy xung quanh mà không tham gia. Đây chính là điểm mấu chốt tạo nên tính chất hóa học đặc trưng cho các hợp chất chứa nitơ và oxy.
Bí quyết chuyên gia: Khi vẽ liên kết cho nhận, hãy tưởng tượng Nitơ giống như một người đầu bếp đang chia sẻ phần thức ăn dư. Sự chia sẻ này không đòi hỏi đối phương phải đáp lại bằng nguyên liệu nào nhưng vẫn tạo ra sự gắn kết.
Cách chuyển đổi sang công thức Lewis của HNO3 chuyên sâu
Để việc quan sát hno3 công thức cấu tạo trở nên dễ dàng hơn, chúng ta chuyển sang dạng công thức Lewis tối giản. Phương pháp phổ biến nhất là thay thế mỗi cặp electron dùng chung bằng một gạch nối đơn giản giữa hai nguyên tử. Một gạch nối tương ứng với liên kết đơn, trong khi hai gạch nối biểu diễn một liên kết đôi mạnh mẽ hơn hẳn. Cách trình bày này giúp các nhà khoa học nhanh chóng nhìn ra khung xương của toàn bộ cấu trúc phân tử phức tạp.
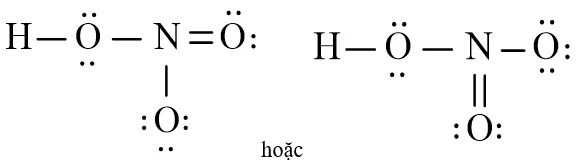 Chuyển đổi từ sơ đồ electron sang công thức Lewis của HNO3Việc thay thế các cặp chấm bằng gạch nối giúp công thức trở nên thoáng đãng và dễ đọc hơn.
Chuyển đổi từ sơ đồ electron sang công thức Lewis của HNO3Việc thay thế các cặp chấm bằng gạch nối giúp công thức trở nên thoáng đãng và dễ đọc hơn.
Trong công thức Lewis, liên kết cho – nhận thường được biểu diễn đặc biệt bằng một mũi tên hướng về phía nguyên tử nhận. Mũi tên này bắt đầu từ nguyên tử Nitơ và hướng thẳng tới nguyên tử Oxy thứ ba mà chúng ta đã phân tích. Cách ký hiệu này giúp người học phân biệt rõ ràng giữa liên kết cộng hóa trị thông thường và liên kết phối trí. Nắm vững điều này, bạn sẽ không bao giờ nhầm lẫn khi làm các bài kiểm tra về hno3 công thức cấu tạo.
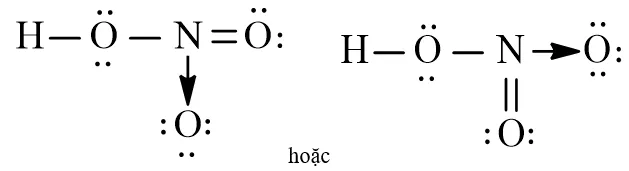 Biểu diễn liên kết phối trí bằng mũi tên trong cấu trúc LewisSử dụng mũi tên để chỉ rõ bản chất của liên kết cho nhận giữa Nitơ trung tâm và Oxy.
Biểu diễn liên kết phối trí bằng mũi tên trong cấu trúc LewisSử dụng mũi tên để chỉ rõ bản chất của liên kết cho nhận giữa Nitơ trung tâm và Oxy.
Hướng dẫn 4 bước vẽ khung cấu trúc phân tử nhanh chóng
Nếu bạn không muốn tính toán chi tiết từng electron, hãy áp dụng quy trình vẽ hno3 công thức cấu tạo 4 bước. Bước một, tính tổng số electron hóa trị của cả phân tử, ở đây chính là con số 24 mà ta đã biết. Bước hai, xác định nguyên tử trung tâm là Nitơ do nó có khả năng tạo nhiều liên kết nhất trong nhóm này. Sau đó, bạn sắp xếp các nguyên tử Oxy xung quanh và đặt nguyên tử Hydro liên kết với một trong các Oxy.
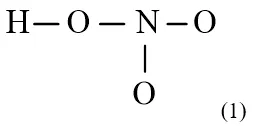 Thiết lập khung xương cơ bản cho phân tử nitric acidKhung xương ban đầu của phân tử trước khi điền đầy đủ các electron hóa trị còn lại.
Thiết lập khung xương cơ bản cho phân tử nitric acidKhung xương ban đầu của phân tử trước khi điền đầy đủ các electron hóa trị còn lại.
Bước ba trong việc vẽ hno3 công thức cấu tạo chính là điền các electron còn lại để đạt bát tử cho Oxy. Sau khi tạo các liên kết đơn cơ bản, bạn còn dư 16 electron để phân bổ vào các vị trí trống của Oxy. Lúc này, bạn sẽ nhận thấy nguyên tử Nitơ trung tâm vẫn chỉ mới có 6 electron, chưa đạt đủ mức 8 cần thiết. Để giải quyết vấn đề này, chúng ta cần chuyển sang bước cuối cùng là tạo thêm các liên kết đa quan trọng.
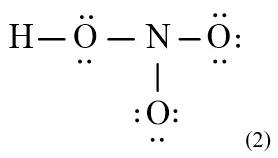 Hoàn thiện các cặp electron tự do trên các nguyên tử Oxy xung quanhTình trạng phân tử khi các nguyên tử Oxy đã đạt bát tử nhưng Nitơ trung tâm vẫn còn thiếu.
Hoàn thiện các cặp electron tự do trên các nguyên tử Oxy xung quanhTình trạng phân tử khi các nguyên tử Oxy đã đạt bát tử nhưng Nitơ trung tâm vẫn còn thiếu.
Bước bốn, bạn thực hiện chuyển một cặp electron chưa liên kết của một nguyên tử Oxy thành một liên kết đôi với Nitơ. Thao tác này giúp nguyên tử Nitơ đạt được quy tắc octet mà không làm thay đổi tổng số electron của toàn phân tử. Kết quả cuối cùng là một bản vẽ hno3 công thức cấu tạo hoàn hảo, chuẩn xác theo mọi giáo trình hóa học hiện đại. Sự luân chuyển electron này đảm bảo tính ổn định về mặt năng lượng cho toàn bộ cấu trúc phân tử axit nitric.
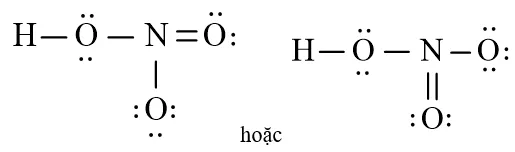 Công thức Lewis hoàn chỉnh sau khi thực hiện các bước tối ưu hóa liên kếtHình ảnh cuối cùng của công thức Lewis phản ánh chính xác trạng thái liên kết của HNO3.
Công thức Lewis hoàn chỉnh sau khi thực hiện các bước tối ưu hóa liên kếtHình ảnh cuối cùng của công thức Lewis phản ánh chính xác trạng thái liên kết của HNO3.
Phân tích bản chất liên kết cộng hóa trị trong HNO3
Khi nhìn vào hno3 công thức cấu tạo, chúng ta cần chú ý đến độ âm điện của các nguyên tử tham gia. Hiệu độ âm điện giữa Nitơ và Oxy là khoảng 0,4, khiến liên kết này mang tính cộng hóa trị phân cực rõ rệt. Các electron dùng chung sẽ bị lệch về phía nguyên tử Oxy do nó có sức hút electron mạnh hơn so với Nitơ. Tương tự, liên kết giữa Oxy và Hydro cũng bị phân cực mạnh về phía Oxy với hiệu độ âm điện lên tới 1,24.
Chính sự phân cực này trong hno3 công thức cấu tạo đã giải thích tính axit đặc trưng của phân tử này trong nước. Liên kết O-H bị yếu đi dưới tác động của điện trường, khiến nguyên tử Hydro dễ dàng tách ra thành ion H+. Khả năng giải phóng ion H+ càng lớn thì nồng độ axit càng cao, tạo nên sức mạnh cho dung dịch nitric acid. Đây là lý do tại sao bạn phải cực kỳ cẩn thận khi thực hiện các thí nghiệm liên quan đến loại axit này.
Cách xác định hno3 công thức cấu tạo từ thực tế liên kết
Từ công thức Lewis hoàn chỉnh, chúng ta có thể dễ dàng suy ra dạng công thức cấu tạo thu gọn nhất hiện nay. Quy tắc là lược bỏ toàn bộ các cặp electron tự do và chỉ giữ lại các gạch nối biểu diện liên kết hóa học. Trong hno3 công thức cấu tạo này, bạn sẽ thấy rõ một liên kết đôi N=O và hai liên kết đơn N-O và O-H. Tổng số liên kết xung quanh nguyên tử Nitơ trung tâm sẽ gợi ý cho bạn về hóa trị thực tế của nó.
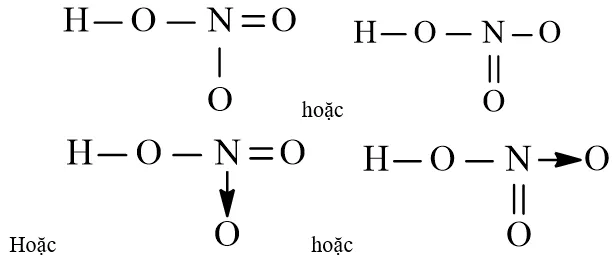 Sơ đồ công thức cấu tạo dạng rút gọn của axit nitricDạng biểu diễn đơn giản nhất thường được sử dụng trong các phương trình phản ứng hóa học.
Sơ đồ công thức cấu tạo dạng rút gọn của axit nitricDạng biểu diễn đơn giản nhất thường được sử dụng trong các phương trình phản ứng hóa học.
Việc nắm vững hno3 công thức cấu tạo còn giúp bạn xác định được các loại liên kết sigma và liên kết pi trong phân tử. Mỗi liên kết đơn tương ứng với một liên kết sigma bền vững, được hình thành từ sự chồng lấn trục giữa các obitan. Liên kết đôi bao gồm một liên kết sigma và một liên kết pi kém bền hơn, dễ dàng tham gia vào các phản ứng. Tổng cộng trong một phân tử HNO3 sẽ tồn tại 4 liên kết sigma và duy nhất một liên kết pi quan trọng.
Bài tập minh họa về cấu trúc phân tử HNO3 năm 2026
Để củng cố kiến thức về hno3 công thức cấu tạo, Chef Kim mời bạn tham khảo một vài câu hỏi trắc nghiệm thực tế. Những câu hỏi này giúp bạn ôn tập nhanh và ghi nhớ sâu các đặc điểm quan trọng về liên kết hóa học.
Câu hỏi 1: Hãy cho biết tổng số liên kết sigma và liên kết pi có trong một phân tử HNO3 đơn lẻ là bao nhiêu?
- A. 3 sigma và 1 pi
- B. 4 sigma và 2 pi
- C. 5 sigma và 0 pi
- D. 4 sigma và 1 pi
Hướng dẫn giải: Dựa vào hno3 công thức cấu tạo, ta thấy có 3 liên kết đơn (O-H, N-O, N→O) và một liên kết đôi (N=O). Liên kết đơn là 1 sigma, liên kết đôi gồm 1 sigma và 1 pi. Vậy đáp án chính xác là D (4 liên kết sigma và 1 liên kết pi).
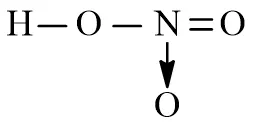 Phân tích hóa trị của Nitơ thông qua cấu trúc phân tử thực tếThông qua cấu tạo, học sinh có thể dễ dàng tính toán được hóa trị và số oxy hóa.
Phân tích hóa trị của Nitơ thông qua cấu trúc phân tử thực tếThông qua cấu tạo, học sinh có thể dễ dàng tính toán được hóa trị và số oxy hóa.
Câu hỏi 2: Hóa trị của nguyên tử Nitơ trong hợp chất axit nitric khi xét theo số liên kết tạo thành là bao nhiêu?
- A. 3
- B. 4
- C. 5
- D. 2
Hướng dẫn giải: Nhìn vào hno3 công thức cấu tạo, nguyên tử Nitơ tạo ra tổng cộng 4 gạch nối liên kết với các nguyên tử Oxy. Do đó, hóa trị của Nitơ trong trường hợp này được xác định là 4, thay vì 5 như nhiều người lầm tưởng. Điều này chứng minh rằng cấu trúc Lewis mang lại cái nhìn chính xác hơn nhiều so với cách tính hóa trị thông thường.
Ứng dụng thực tiễn của kiến thức về cấu tạo HNO3
Tại nhà hàng Korea House, chúng tôi luôn coi trọng việc hiểu biết về hóa học để đảm bảo vệ sinh an toàn thực phẩm. Dù nitric acid không dùng trong nấu ăn, nhưng các dẫn xuất của nó như muối nitrate lại có vai trò bảo quản. Khi bạn hiểu hno3 công thức cấu tạo, bạn sẽ biết cách các nhóm chức này tương tác với protein trong các loại thịt. Kiến thức khoa học giúp người đầu bếp làm chủ được quá trình lên men và giữ màu sắc tự nhiên cho thực phẩm.
Bên cạnh đó, việc hiểu rõ cấu tạo hóa học còn giúp chúng ta lựa chọn các chất tẩy rửa nhà bếp an toàn. Nhiều loại dung dịch tẩy mạnh có thành phần gốc nitơ cần được sử dụng đúng nồng độ để không gây hỏng bề mặt inox. hno3 công thức cấu tạo phân cực mạnh cho thấy nó tan rất tốt trong nước, nhưng lại cực kỳ háu nước và tỏa nhiệt. Do đó, hãy luôn nhớ quy tắc “cho axit vào nước” để đảm bảo an toàn tuyệt đối khi phải pha chế dung dịch.
Lưu ý an toàn từ Chef Kim: Tuyệt đối không bao giờ để các chất có gốc axit tiếp xúc trực tiếp với da hoặc mắt của bạn. Sự hiểu biết về cấu hình electron và liên kết hóa học chính là tấm khiên bảo vệ bạn trong mọi tình huống thực tế.
Hi vọng rằng bài viết chi tiết này đã giúp bạn hoàn toàn làm chủ cách vẽ hno3 công thức cấu tạo trong chương trình mới. Sự kết hợp giữa lý thuyết hóa học chuẩn xác và những mẹo nhỏ thực tế sẽ làm cho việc học trở nên thú vị hơn. Đừng quên theo dõi blog của Korea House để cập nhật thêm nhiều hướng dẫn bổ ích về nấu ăn và khoa học 2026. Chúc bạn luôn giữ được lửa đam mê với những kiến thức mới mỗi ngày trên hành trình khám phá thế giới xung quanh.
Ngày cập nhật mới nhất 01/03/2026 by Chef Kim
Chef Kim là người phụ trách phát triển hương vị và nội dung ẩm thực tại Korea House – Delivery Korea Food. Với kinh nghiệm trực tiếp trong bếp và sự am hiểu các món ăn Hàn Quốc quen thuộc, Chef Kim tập trung chia sẻ cách chế biến đơn giản, nguyên liệu dễ tìm và hương vị phù hợp khẩu vị người Việt, dựa trên quá trình nấu thử và phản hồi thực tế từ khách hàng.
