Viết công thức Lewis của SO₃ là một trong những dạng bài tập quan trọng trong chương trình Hóa học phổ thông. Bài viết này sẽ hướng dẫn bạn cách viết công thức electron, công thức Lewis và công thức cấu tạo của phân tử lưu huỳnh trioxide một cách chính xác và dễ hiểu nhất.
Phân Tích Cấu Hình Electron và Khả Năng Liên Kết
Trước khi viết công thức Lewis của SO₃, cần hiểu rõ cấu hình electron của các nguyên tố tham gia:
Nguyên tử lưu huỳnh (S):
- Cấu hình electron: 1s²2s²2p⁶3s²3p⁴
- Có 6 electron hóa trị ở lớp ngoài cùng
- Cần thêm 2 electron để đạt cấu hình bền vững của khí hiếm
Nguyên tử oxygen (O):
- Cấu hình electron: 1s²2s²2p⁴
- Có 6 electron hóa trị
- Cần thêm 2 electron để hoàn thành octet
Trong phân tử SO₃, nguyên tử S đóng vai trò trung tâm do có độ âm điện nhỏ hơn (2,58 so với 3,44 của O). Ba nguyên tử oxygen sẽ bao quanh nguyên tử lưu huỳnh.
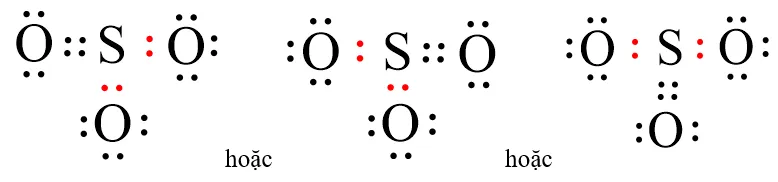 Cấu trúc phân tử SO3 với nguyên tử S ở trung tâmSơ đồ electron của phân tử SO₃ thể hiện các cặp electron liên kết và tự do
Cấu trúc phân tử SO3 với nguyên tử S ở trung tâmSơ đồ electron của phân tử SO₃ thể hiện các cặp electron liên kết và tự do
Cách Viết Công Thức Electron của SO₃
Quá trình hình thành liên kết trong phân tử SO₃ diễn ra theo các bước:
Bước 1: Tạo liên kết đôi S=O
Nguyên tử S và một nguyên tử O góp chung 2 electron để tạo thành 2 cặp electron dùng chung (liên kết đôi). Lúc này cả S và O đều đạt octet.
Bước 2: Tạo liên kết cho-nhận với hai O còn lại
Hai nguyên tử O còn lại chưa đạt octet. Nguyên tử S sử dụng một cặp electron tự do làm cặp electron chung với mỗi nguyên tử O. Đây là liên kết cho-nhận, trong đó:
- S là nguyên tử cho (đóng góp cặp electron)
- O là nguyên tử nhận (không đóng góp electron)
Công thức electron hoàn chỉnh:
Phân tử SO₃ có:
- 4 cặp electron chung (2 cặp từ liên kết đôi S=O, 2 cặp từ liên kết cho-nhận)
- 8 cặp electron tự do thuộc các nguyên tử O
- Nguyên tử S không còn electron tự do
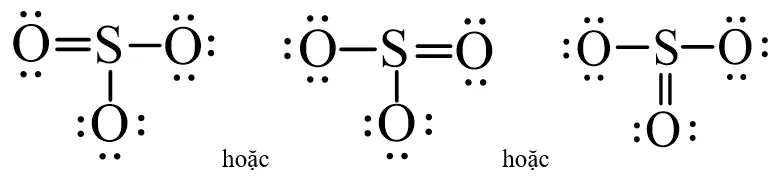 Công thức electron của SO3Công thức electron của SO₃ với các cặp electron được biểu diễn bằng dấu chấm
Công thức electron của SO3Công thức electron của SO₃ với các cặp electron được biểu diễn bằng dấu chấm
Hai Phương Pháp Viết Công Thức Lewis của SO₃
Phương pháp 1: Chuyển đổi từ công thức electron
Thay mỗi cặp electron dùng chung bằng một gạch nối (-) giữa hai nguyên tử. Các cặp electron tự do vẫn giữ nguyên dạng dấu chấm.
Công thức Lewis cơ bản:
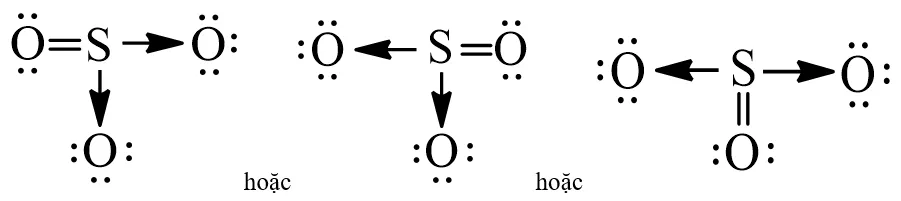 Công thức Lewis của SO3 dạng cơ bảnCông thức Lewis của SO₃ với liên kết cho-nhận được biểu diễn bằng mũi tên
Công thức Lewis của SO3 dạng cơ bảnCông thức Lewis của SO₃ với liên kết cho-nhận được biểu diễn bằng mũi tên
Để thể hiện rõ liên kết cho-nhận, thay cặp electron chỉ do S đóng góp bằng mũi tên từ nguyên tử cho (S) đến nguyên tử nhận (O).
Phương pháp 2: Áp dụng quy tắc octet
Bước 1: Tính tổng electron hóa trị
Tổng electron hóa trị = 6 (của S) + 6×3 (của 3 O) = 24 electron
Bước 2: Vẽ khung phân tử với liên kết đơn
Sơ đồ khung phân tử SO₃ với các liên kết đơn ban đầu
Số electron đã dùng: 2×3 = 6 electron Số electron còn lại: 24 – 6 = 18 electron
Bước 3: Hoàn thành octet cho các nguyên tử O
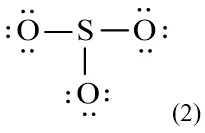 Hoàn thành octet cho oxygenBổ sung electron tự do cho các nguyên tử oxygen
Hoàn thành octet cho oxygenBổ sung electron tự do cho các nguyên tử oxygen
Mỗi O cần thêm 6 electron (3 cặp) để đạt octet. Số electron còn lại: 18 – 18 = 0
Lúc này nguyên tử S chỉ có 6 electron, chưa đạt octet.
Bước 4: Tạo liên kết bội
Chuyển một cặp electron tự do từ một nguyên tử O thành cặp electron dùng chung với S để S đạt octet.
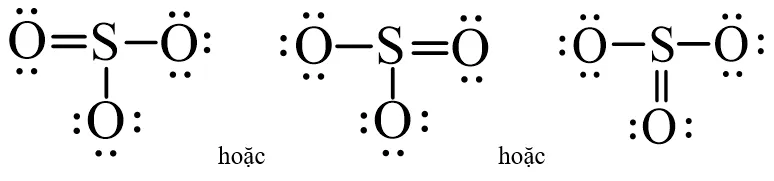 Công thức Lewis hoàn chỉnh của SO3Công thức Lewis hoàn chỉnh của SO₃ sau khi tạo liên kết đôi
Công thức Lewis hoàn chỉnh của SO3Công thức Lewis hoàn chỉnh của SO₃ sau khi tạo liên kết đôi
Đặc Điểm Cấu Trúc và Liên Kết
Phân tích độ phân cực:
Hiệu độ âm điện: Δχ(S-O) = |2,58 – 3,44| = 0,86
Vì 0,4 < 0,86 < 1,7 nên liên kết S-O trong SO₃ là liên kết cộng hóa trị phân cực, phân cực về phía nguyên tử O.
Hình dạng phân tử:
Phân tử SO₃ có cấu trúc tam giác phẳng với:
- Góc liên kết O-S-O = 120°
- Nguyên tử S nằm ở tâm
- Ba nguyên tử O nằm ở ba đỉnh của tam giác đều
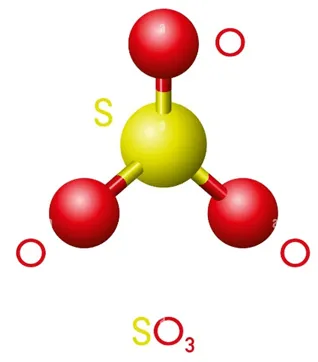 Cấu trúc tam giác phẳng của SO3Mô hình không gian của phân tử SO₃ dạng tam giác phẳng
Cấu trúc tam giác phẳng của SO3Mô hình không gian của phân tử SO₃ dạng tam giác phẳng
Công Thức Cấu Tạo của SO₃
Từ công thức Lewis, loại bỏ các electron tự do (electron không tham gia liên kết) để thu được công thức cấu tạo.
Hai cách biểu diễn:
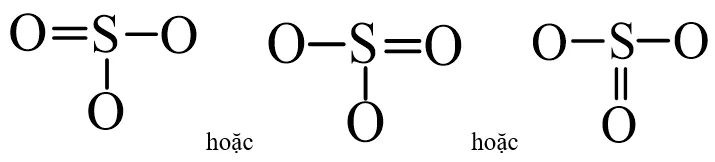 Công thức cấu tạo SO3 dạng 1Công thức cấu tạo của SO₃ thể hiện một liên kết đôi và hai liên kết đơn
Công thức cấu tạo SO3 dạng 1Công thức cấu tạo của SO₃ thể hiện một liên kết đôi và hai liên kết đơn
Hoặc sử dụng mũi tên để thể hiện liên kết cho-nhận:
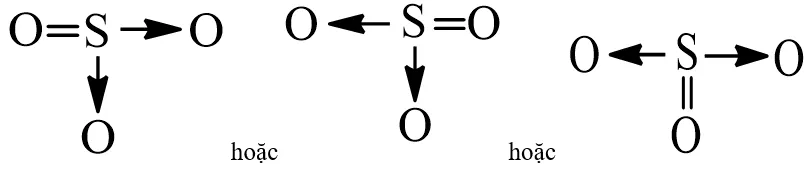 Công thức cấu tạo SO3 dạng 2Công thức cấu tạo của SO₃ với liên kết cho-nhận được biểu diễn bằng mũi tên
Công thức cấu tạo SO3 dạng 2Công thức cấu tạo của SO₃ với liên kết cho-nhận được biểu diễn bằng mũi tên
Trong phân tử SO₃:
- Có một liên kết đôi S=O (do S và O cùng góp electron)
- Có hai liên kết đơn S→O (liên kết cho-nhận, chỉ S góp electron)
Bài Tập Vận Dụng
Câu 1: Công thức biểu diễn cấu trúc Lewis của phân tử SO₃ là:
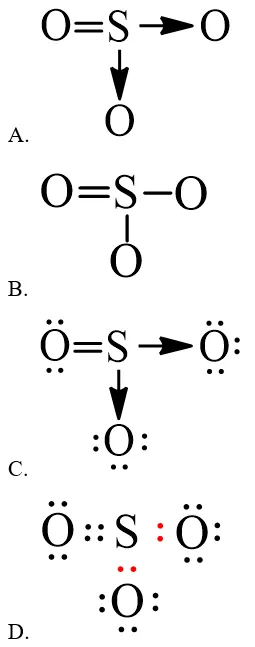 Các đáp án về công thức Lewis của SO3Bốn phương án lựa chọn cho công thức Lewis của SO₃
Các đáp án về công thức Lewis của SO3Bốn phương án lựa chọn cho công thức Lewis của SO₃
Đáp án: C
Giải thích: Công thức Lewis phải thể hiện đầy đủ cả electron liên kết và electron tự do. Đáp án A, B chỉ là công thức cấu tạo (không có electron tự do). Đáp án D là công thức electron (dùng dấu chấm thay vì gạch nối).
Câu 2: Trong phân tử SO₃, số cặp electron chỉ do nguyên tử S đóng góp (liên kết cho-nhận) là:
A. 1
B. 2
C. 3
D. 4
Đáp án: B
Giải thích: Khi tạo phân tử SO₃:
- S và một O góp chung electron tạo liên kết đôi (không phải liên kết cho-nhận)
- S đóng góp một cặp electron cho mỗi trong hai O còn lại
- Tổng cộng có 2 liên kết cho-nhận
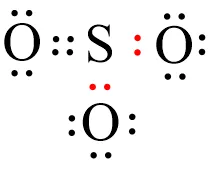 Minh họa liên kết cho-nhận trong SO3Sơ đồ thể hiện hai liên kết cho-nhận trong phân tử SO₃
Minh họa liên kết cho-nhận trong SO3Sơ đồ thể hiện hai liên kết cho-nhận trong phân tử SO₃
Mẹo ghi nhớ: Trong SO₃, nguyên tử S “cho” 2 cặp electron và “nhận” 2 cặp electron từ một O, tạo nên cấu trúc đối xứng tam giác phẳng.
Nắm vững cách viết công thức Lewis của SO₃ sẽ giúp bạn dễ dàng áp dụng cho các phân tử phức tạp khác như SO₂, H₂SO₄, NH4+, hay các hợp chất chứa liên kết cho-nhận.
Ngày cập nhật mới nhất 14/03/2026 by Chef Kim
Chef Kim là người phụ trách phát triển hương vị và nội dung ẩm thực tại Korea House – Delivery Korea Food. Với kinh nghiệm trực tiếp trong bếp và sự am hiểu các món ăn Hàn Quốc quen thuộc, Chef Kim tập trung chia sẻ cách chế biến đơn giản, nguyên liệu dễ tìm và hương vị phù hợp khẩu vị người Việt, dựa trên quá trình nấu thử và phản hồi thực tế từ khách hàng.
