Công thức Lewis của NH4Cl thể hiện cấu trúc electron của muối amoni clorua, giúp hiểu rõ bản chất liên kết giữa các nguyên tử trong hợp chất ion này. Bài viết hướng dẫn chi tiết cách viết công thức Lewis NH4Cl theo phương pháp khoa học, phù hợp với chương trình hóa học phổ thông.
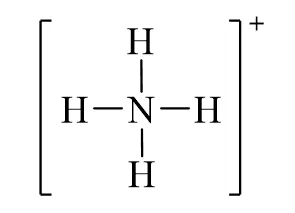 Công thức Lewis của NH4Cl
Công thức Lewis của NH4Cl
Bản chất cấu trúc của NH4Cl
NH4Cl là hợp chất ion được tạo thành từ cation NH4+ và anion Cl-. Để viết công thức Lewis NH4Cl chính xác, cần hiểu rõ cấu trúc từng ion thành phần.
Trong NH4Cl, liên kết ion hình thành do lực hút tĩnh điện giữa ion dương NH4+ và ion âm Cl-. Tuy nhiên, bên trong cation NH4+, các nguyên tử liên kết với nhau bằng liên kết cộng hóa trị có cực, trong đó có một liên kết phối trí đặc biệt.
Cách viết công thức Lewis của ion NH4+
Xác định tổng số electron hóa trị
Nguyên tử nitơ (N) thuộc nhóm VA có 5 electron hóa trị. Mỗi nguyên tử hydro (H) có 1 electron hóa trị. Ion NH4+ mang điện tích +1, nghĩa là đã mất đi 1 electron so với phân tử trung hòa.
Tổng số electron hóa trị = 5 + (1 × 4) – 1 = 8 electron.
Con số 8 này cho thấy ion NH4+ có đủ electron để tạo 4 liên kết đơn mà không còn cặp electron tự do nào trên nguyên tử trung tâm.
Vẽ khung phân tử với liên kết đơn
Nitơ đóng vai trò nguyên tử trung tâm vì có độ âm điện lớn hơn hydro và khả năng tạo nhiều liên kết hơn. Bốn nguyên tử H được sắp xếp đối xứng xung quanh N, mỗi liên kết N-H tiêu tốn 2 electron.
Cấu trúc này tạo nên hình học tứ diện đều, với góc liên kết H-N-H xấp xỉ 109,5°.
Phân bổ electron còn lại
Sau khi tạo 4 liên kết đơn, số electron đã sử dụng là 4 × 2 = 8 electron. So với tổng số electron hóa trị ban đầu (8 electron), không còn electron nào chưa được phân bổ.
Mỗi nguyên tử H đạt cấu hình bền vững với 2 electron (quy tắc duet). Nguyên tử N đạt octet với 8 electron xung quanh (4 cặp electron liên kết).
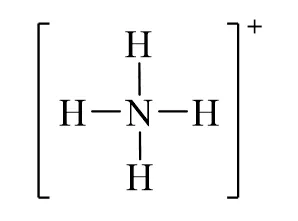 Công thức Lewis của NH4Cl
Công thức Lewis của NH4Cl
Đặc điểm liên kết trong NH4+
Ba trong bốn liên kết N-H được hình thành theo cơ chế liên kết cộng hóa trị thông thường, mỗi nguyên tử đóng góp 1 electron. Liên kết thứ tư là liên kết phối trí, trong đó cặp electron dùng chung hoàn toàn do nguyên tử N cung cấp.
Sau khi hình thành, cả bốn liên kết N-H trong NH4+ đều có bản chất và độ dài tương đương nhau. Không thể phân biệt liên kết nào là liên kết phối trí dựa vào cấu trúc hoặc tính chất hóa học.
Liên kết giữa N và H trong NH4+ là liên kết cộng hóa trị có cực do sự chênh lệch độ âm điện giữa hai nguyên tố (N: 3,04; H: 2,20). Mật độ electron lệch về phía nguyên tử nitơ, tạo nên cực âm một phần trên N và cực dương một phần trên H.
Công thức Lewis hoàn chỉnh của NH4Cl
Công thức Lewis NH4Cl được biểu diễn bằng cách đặt cấu trúc Lewis của NH4+ cạnh ion Cl-, kèm theo dấu điện tích tương ứng. Ion Cl- có 8 electron hóa trị (7 electron của Cl trung hòa cộng thêm 1 electron nhận được), được biểu diễn dưới dạng 4 cặp electron tự do xung quanh nguyên tử clo.
Lực hút tĩnh điện giữa ion NH4+ mang điện tích dương và ion Cl- mang điện tích âm tạo nên liên kết ion, giữ cho cấu trúc tinh thể NH4Cl ổn định ở điều kiện thường.
Ứng dụng thực tế của công thức Lewis
Công thức Lewis giúp dự đoán hình học phân tử và tính chất vật lý của hợp chất. Với NH4Cl, cấu trúc tứ diện của ion NH4+ giải thích tính tan tốt trong nước do khả năng tạo liên kết hydro với các phân tử H2O.
Hiểu rõ công thức Lewis NH4Cl còn hỗ trợ việc giải thích phản ứng nhiệt phân của muối amoni, trong đó liên kết ion bị phá vỡ tạo thành NH3 và HCl khí khi đun nóng.
Câu hỏi vận dụng
Câu 1. Liên kết giữa nguyên tử H và nguyên tử N trong NH4+ là loại liên kết gì?
A. Liên kết hydrogen
B. Liên kết cộng hóa trị có cực
C. Liên kết cộng hóa trị không cực
D. Liên kết ion
Đáp án đúng: B
Liên kết N-H trong NH4+ là liên kết cộng hóa trị có cực do sự chênh lệch độ âm điện giữa nitơ và hydro. Mặc dù một trong bốn liên kết được hình thành theo cơ chế phối trí, bản chất của tất cả các liên kết N-H đều là cộng hóa trị có cực.
Nắm vững cách viết công thức Lewis NH4Cl giúp học sinh hiểu sâu về bản chất liên kết hóa học, từ đó áp dụng hiệu quả vào các bài tập về cấu trúc phân tử và dự đoán tính chất hợp chất.
Ngày cập nhật mới nhất 17/03/2026 by Chef Kim
Chef Kim là người phụ trách phát triển hương vị và nội dung ẩm thực tại Korea House – Delivery Korea Food. Với kinh nghiệm trực tiếp trong bếp và sự am hiểu các món ăn Hàn Quốc quen thuộc, Chef Kim tập trung chia sẻ cách chế biến đơn giản, nguyên liệu dễ tìm và hương vị phù hợp khẩu vị người Việt, dựa trên quá trình nấu thử và phản hồi thực tế từ khách hàng.
