Công thức cấu tạo của C₃H₈ là CH₃-CH₂-CH₃, đại diện cho propan – hydrocarbon no mạch thẳng đơn giản nhất trong họ ankan có 3 nguyên tử carbon. Khác với các đồng đẳng cao hơn như butan (C₄H₁₀) hay pentan (C₅H₁₂), propan không tồn tại đồng phân mạch cacbon do cấu trúc phân tử quá ngắn. Bài viết này phân tích chi tiết cấu trúc, tính chất và ứng dụng thực tế của propan trong đời sống.
Phân Tích Cấu Trúc Phân Tử C₃H₈
Độ Bất Bão Hòa Và Đặc Điểm Liên Kết
Áp dụng công thức tính độ bất bão hòa:
k = (2C + 2 – H) / 2 = (2×3 + 2 – 8) / 2 = 0
Kết quả k = 0 chứng tỏ phân tử propan:
- Không chứa liên kết đôi (π)
- Không chứa vòng cacbon
- Chỉ có liên kết đơn (σ) giữa các nguyên tử
- Thuộc nhóm hydrocarbon no (ankan)
Đây là đặc trưng của ankan – họ hợp chất bão hòa với công thức tổng quát CₙH₂ₙ₊₂.
Cấu Trúc Hình Học Không Gian
Propan có cấu trúc không gian đặc biệt:
- Mỗi nguyên tử C lai hóa sp³
- Góc liên kết C-C-C ≈ 109.5° (tứ diện)
- Chiều dài liên kết C-C: 1.54 Å
- Chiều dài liên kết C-H: 1.09 Å
Cấu trúc này tạo nên hình dạng zigzag đặc trưng của mạch cacbon no.
Công Thức Cấu Tạo Của C₃H₈ Chi Tiết
Biểu Diễn Cấu Trúc
| Loại công thức | Biểu diễn | Đặc điểm |
|---|---|---|
| Công thức phân tử | C₃H₈ | Thành phần nguyên tố |
| Công thức cấu tạo thu gọn | CH₃-CH₂-CH₃ | Thứ tự liên kết các nguyên tử |
| Công thức cấu tạo đầy đủ | H₃C-CH₂-CH₃ (với tất cả H) | Hiển thị mọi liên kết |
| Công thức bán khai triển | CH₃CH₂CH₃ | Dạng viết gọn nhất |
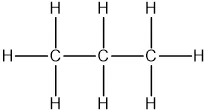 Công thức cấu tạo của propan C₃H₈ với mạch cacbon thẳng và các nguyên tử hydro liên kết
Công thức cấu tạo của propan C₃H₈ với mạch cacbon thẳng và các nguyên tử hydro liên kết
Phân Tích Từng Vị Trí Carbon
Carbon đầu mạch (C₁ và C₃):
- Liên kết với 3 nguyên tử H
- Liên kết với 1 nguyên tử C
- Gọi là carbon bậc 1 (primary carbon)
Carbon giữa mạch (C₂):
- Liên kết với 2 nguyên tử H
- Liên kết với 2 nguyên tử C
- Gọi là carbon bậc 2 (secondary carbon)
Tại Sao C₃H₈ Không Có Đồng Phân?
Giải Thích Về Đồng Phân Mạch Cacbon
Đồng phân mạch cacbon xuất hiện khi có thể sắp xếp các nguyên tử C theo nhiều cách khác nhau. Với propan:
Mạch thẳng duy nhất: C-C-C
- Đây là cách sắp xếp duy nhất cho 3 nguyên tử carbon
- Không thể tạo mạch nhánh vì cần tối thiểu 4 carbon
So sánh với butan (C₄H₁₀):
- Butan có 2 đồng phân: n-butan (CH₃-CH₂-CH₂-CH₃) và isobutan (CH₃-CH(CH₃)-CH₃)
- Từ C₄ trở lên mới xuất hiện đồng phân mạch
Quy Tắc Chung Về Đồng Phân Ankan
| Số carbon | Số đồng phân | Ví dụ |
|---|---|---|
| C₁ – C₃ | 1 | Metan, etan, propan |
| C₄ | 2 | n-butan, isobutan |
| C₅ | 3 | n-pentan, isopentan, neopentan |
| C₆ | 5 | Các đồng phân hexan |
| C₁₀ | 75 | Phức tạp |
Cách Gọi Tên C₃H₈ Theo Chuẩn IUPAC
Danh Pháp Quốc Tế
Tên IUPAC: Propan (Propane)
Cách đặt tên:
- Đếm số carbon mạch chính: 3 carbon → tiền tố “prop-“
- Xác định loại liên kết: chỉ có liên kết đơn → hậu tố “-an”
- Kết hợp: Prop + an = Propan
Tên Gọi Khác
- Tên thông thường: Propan (giống IUPAC)
- Tên thương mại: LPG (Liquefied Petroleum Gas) khi pha trộn với butan
- Tên hóa học cũ: Không có tên thay thế
Mẹo ghi nhớ: Tiền tố “prop-” xuất phát từ tiếng Hy Lạp “protos” (đầu tiên) + “pion” (béo), ám chỉ ankan đầu tiên có 3 carbon.
Tính Chất Vật Lý Của Propan
Đặc Điểm Quan Sát Được
- Trạng thái: Khí không màu ở điều kiện thường
- Mùi: Không mùi tự nhiên (thêm chất tạo mùi để phát hiện rò rỉ)
- Nhiệt độ sôi: -42°C (dễ hóa lỏng)
- Nhiệt độ nóng chảy: -188°C
- Khối lượng riêng: 0.493 g/cm³ (ở -45°C, thể lỏng)
- Độ tan: Không tan trong nước, tan trong dung môi hữu cơ
Tính Chất Đặc Biệt
Dễ hóa lỏng: Ở áp suất 8-10 atm (nhiệt độ thường), propan chuyển sang thể lỏng. Đây là cơ sở để nén propan vào bình gas.
Nặng hơn không khí: Khối lượng phân tử 44 g/mol > không khí (29 g/mol) → propan rò rỉ sẽ tụ ở chỗ thấp, nguy hiểm cháy nổ.
Tính Chất Hóa Học Và Phản Ứng Đặc Trưng
Phản Ứng Cháy (Quan Trọng Nhất)
Phương trình:
C₃H₈ + 5O₂ → 3CO₂ + 4H₂O (ΔH = -2220 kJ/mol)Đặc điểm:
- Tỏa nhiệt mạnh (năng lượng cao)
- Ngọn lửa màu xanh nhạt
- Cháy hoàn toàn khi đủ O₂
- Cháy không hoàn toàn tạo CO (độc) khi thiếu O₂
Phản Ứng Thế Halogen
Với clo (Cl₂) có ánh sáng:
C₃H₈ + Cl₂ → C₃H₇Cl + HCl (1-clopropan hoặc 2-clopropan)
C₃H₇Cl + Cl₂ → C₃H₆Cl₂ + HCl (diclopropan)Tạo hỗn hợp sản phẩm do có 2 vị trí H khác nhau (H ở C đầu mạch và C giữa mạch).
Phản Ứng Cracking (Nhiệt Phân)
Ở nhiệt độ cao (500-700°C), xúc tác:
C₃H₈ → C₂H₄ + CH₄ (etilen + metan)
C₃H₈ → C₃H₆ + H₂ (propen + hydro)Ứng dụng: Sản xuất etilen làm nguyên liệu công nghiệp hóa dầu.
Ứng Dụng Thực Tế Của Propan
Nhiên Liệu Dân Dụng
Gas nấu ăn (LPG):
- Thành phần: 60-70% propan + 30-40% butan
- Ưu điểm: Cháy sạch, nhiệt lượng cao (≈ 46 MJ/kg), dễ vận chuyển
- Bình gas 12kg chứa khoảng 24 lít propan lỏng
Nhiên liệu sưởi ấm:
- Dùng ở vùng lạnh (Bắc Mỹ, châu Âu)
- Hiệu suất cao hơn điện ở vùng xa lưới điện
Công Nghiệp Và Thương Mại
Nguyên liệu hóa dầu:
- Sản xuất propylen (C₃H₆) → nhựa polypropylene
- Tổng hợp hóa chất: acetone, isopropanol
Chất làm lạnh:
- Thay thế CFC trong tủ lạnh, điều hòa (R-290)
- Thân thiện môi trường (GWP thấp)
Khí đẩy (propellant):
- Bình xịt (spray) mỹ phẩm, sơn
- Thay thế các chất gây hại tầng ozone
Ứng Dụng Đặc Biệt
Nhiên liệu xe hơi (Autogas):
- Phổ biến ở châu Âu, châu Á
- Giảm 10-15% khí thải CO₂ so với xăng
- Chi phí thấp hơn xăng 30-40%
Khí bật lửa:
- Propan tinh khiết hoặc pha butan
- Áp suất hơi phù hợp ở nhiệt độ thường
An Toàn Khi Sử Dụng Propan
Nguy Hiểm Tiềm Ẩn
Cháy nổ:
- Giới hạn nổ: 2.1% – 9.5% thể tích trong không khí
- Năng lượng đánh lửa tối thiểu: 0.25 mJ (rất thấp)
Ngạt khí:
- Propan chiếm chỗ oxy trong không gian kín
- Gây thiếu oxy nếu rò rỉ nhiều
Đông lạnh:
- Propan lỏng bay hơi hấp thụ nhiệt → gây bỏng lạnh da
Biện Pháp An Toàn
Quy tắc vàng: Luôn kiểm tra van, ống dẫn gas trước khi sử dụng. Dùng nước xà phòng phát hiện rò rỉ (xuất hiện bọt khí).
Khi sử dụng bình gas:
- Đặt bình thẳng đứng, thoáng khí
- Không để gần nguồn nhiệt, lửa
- Tắt van sau mỗi lần dùng
- Thay bình khi hết gas, không đổ gas tự ý
Khi nghi ngờ rò rỉ:
- Tắt van bình ngay
- Mở cửa thông gió
- Không bật công tắc điện
- Gọi thợ chuyên nghiệp kiểm tra
So Sánh Propan Với Các Ankan Khác
| Đặc điểm | Metan (C₁) | Etan (C₂) | Propan (C₃) | Butan (C₄) |
|---|---|---|---|---|
| Nhiệt độ sôi | -162°C | -89°C | -42°C | -0.5°C |
| Trạng thái (25°C, 1 atm) | Khí | Khí | Khí | Khí |
| Năng lượng cháy (kJ/mol) | 890 | 1560 | 2220 | 2877 |
| Số đồng phân | 1 | 1 | 1 | 2 |
| Ứng dụng chính | Khí đốt tự nhiên | Nguyên liệu etilen | Gas nấu ăn | Gas nấu ăn, bật lửa |
Nhận xét: Propan là điểm cân bằng lý tưởng giữa năng lượng cao và dễ hóa lỏng, phù hợp làm nhiên liệu dân dụng.
Câu Hỏi Thường Gặp
Tại sao gas nấu ăn có mùi dù propan không mùi?
Các nhà sản xuất thêm mercaptan (C₂H₆S) – chất có mùi hôi đặc trưng – để phát hiện rò rỉ gas. Nồng độ mercaptan rất nhỏ (≈ 0.001%) không ảnh hưởng đến quá trình cháy.
Propan và butan khác nhau như thế nào?
- Propan (C₃H₈): Nhiệt độ sôi -42°C, bay hơi tốt ở mùa đông
- Butan (C₄H₁₀): Nhiệt độ sôi -0.5°C, khó bay hơi khi lạnh
- LPG thường pha trộn cả hai để tối ưu hiệu suất theo mùa
Có thể dùng propan thay thế khí tự nhiên không?
Có, nhưng cần điều chỉnh đầu đốt vì propan có áp suất và nhiệt lượng khác khí tự nhiên (chủ yếu là metan). Nhiều thiết bị hiện đại có chế độ chuyển đổi nhiên liệu.
Propan (C₃H₈) với công thức cấu tạo CH₃-CH₂-CH₃ là hydrocarbon đơn giản nhưng vô cùng quan trọng trong đời sống. Từ bếp gas gia đình đến công nghiệp hóa dầu, propan đóng vai trò không thể thay thế nhờ tính chất hóa học ổn định, năng lượng cháy cao và khả năng hóa lỏng dễ dàng. Hiểu rõ cấu trúc và tính chất của propan giúp sử dụng an toàn, hiệu quả nguồn năng lượng này.
Ngày cập nhật mới nhất 09/03/2026 by Chef Kim
Chef Kim là người phụ trách phát triển hương vị và nội dung ẩm thực tại Korea House – Delivery Korea Food. Với kinh nghiệm trực tiếp trong bếp và sự am hiểu các món ăn Hàn Quốc quen thuộc, Chef Kim tập trung chia sẻ cách chế biến đơn giản, nguyên liệu dễ tìm và hương vị phù hợp khẩu vị người Việt, dựa trên quá trình nấu thử và phản hồi thực tế từ khách hàng.
