Viết công thức Lewis của SF6 (lưu huỳnh hexafluoride) là một trong những bài tập quan trọng giúp học sinh hiểu rõ cấu trúc phân tử và liên kết hóa học. Bài viết này sẽ hướng dẫn bạn hai phương pháp viết công thức Lewis của SF6 một cách chính xác và dễ hiểu nhất.
SF6 Là Gì và Tại Sao Cần Viết Công Thức Lewis?
SF6 (sulfur hexafluoride) là hợp chất vô cơ gồm một nguyên tử lưu huỳnh liên kết với sáu nguyên tử flo. Đây là khí trơ, không màu, không mùi, được sử dụng rộng rãi trong công nghiệp điện và y tế.
Công thức Lewis giúp biểu diễn trực quan cách các electron hóa trị được sắp xếp và chia sẻ giữa các nguyên tử trong phân tử. Với SF6, việc nắm vững cách viết công thức Lewis giúp bạn hiểu được:
- Cấu trúc bát diện đặc biệt của phân tử
- Hiện tượng mở rộng octet ở nguyên tử lưu huỳnh
- Bản chất của sáu liên kết S-F
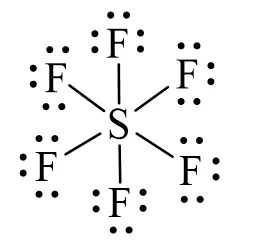 Cấu trúc phân tử SF6 với nguyên tử lưu huỳnh ở trung tâm liên kết với sáu nguyên tử flo
Cấu trúc phân tử SF6 với nguyên tử lưu huỳnh ở trung tâm liên kết với sáu nguyên tử flo
Phương Pháp 1: Viết Công Thức Lewis SF6 Từ Công Thức Electron
Phân Tích Electron Hóa Trị
Trước khi viết công thức Lewis của SF6, cần xác định số electron hóa trị của từng nguyên tố:
- Lưu huỳnh (S): Thuộc nhóm VIA, có 6 electron hóa trị với cấu hình electron lớp ngoài cùng là 3s²3p⁴
- Flo (F): Thuộc nhóm VIIA, có 7 electron hóa trị với cấu hình electron lớp ngoài cùng là 2s²2p⁵
Cơ Chế Hình Thành Liên Kết
Trong phân tử SF6, mỗi nguyên tử flo cần thêm 1 electron để đạt cấu hình bền vững của khí hiếm (octet). Nguyên tử lưu huỳnh ở trung tâm sẽ góp chung electron với cả sáu nguyên tử flo.
Điểm đặc biệt: Lưu huỳnh thuộc chu kỳ 3, có khả năng sử dụng obitan d trống (3d) để mở rộng lớp vỏ hóa trị, chứa được nhiều hơn 8 electron.
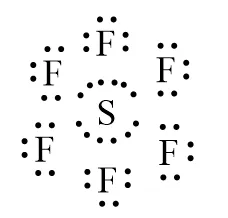 Công thức electron của SF6 thể hiện các cặp electron dùng chung
Công thức electron của SF6 thể hiện các cặp electron dùng chung
Từ Công Thức Electron Đến Công Thức Lewis
Sau khi xác định được công thức electron, ta thay thế mỗi cặp electron dùng chung bằng một gạch nối (đại diện cho liên kết cộng hóa trị đơn).
Mẹo từ Chef Kim: Khi viết công thức Lewis, hãy luôn kiểm tra lại số electron của nguyên tử trung tâm. Với SF6, lưu huỳnh có 12 electron hóa trị (vượt octet) nhưng vẫn bền vững do thuộc chu kỳ 3 trở lên.
Phương Pháp 2: Viết Công Thức Lewis Theo Quy Trình Chuẩn
Bước 1: Tính Tổng Số Electron Hóa Trị
Công thức tính: Tổng electron = (số electron hóa trị của S × số nguyên tử S) + (số electron hóa trị của F × số nguyên tử F)
Áp dụng cho SF6:
- Lưu huỳnh: 6 electron × 1 nguyên tử = 6 electron
- Flo: 7 electron × 6 nguyên tử = 42 electron
- Tổng cộng: 48 electron hóa trị
Bước 2: Vẽ Khung Phân Tử
Xác định nguyên tử trung tâm: Lưu huỳnh có độ âm điện thấp hơn flo (2.58 so với 3.98), nên S đứng ở trung tâm. Sắp xếp sáu nguyên tử F xung quanh S theo cấu trúc bát diện.
Mỗi liên kết đơn S-F sử dụng 2 electron. Với 6 liên kết, ta đã dùng 12 electron.
Bước 3: Phân Bổ Electron Còn Lại
Số electron còn lại: 48 – 12 = 36 electron
Ưu tiên hoàn thành octet cho các nguyên tử flo (nguyên tố có độ âm điện cao hơn):
- Mỗi nguyên tử F cần thêm 6 electron (3 cặp electron tự do) để đạt octet
- Tổng cộng: 6 × 6 = 36 electron
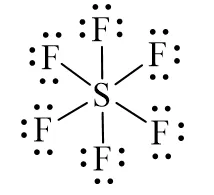 Công thức Lewis đầy đủ của SF6 với các cặp electron tự do trên flo
Công thức Lewis đầy đủ của SF6 với các cặp electron tự do trên flo
Kiểm Tra Công Thức Cuối Cùng
Sau khi phân bổ hết 48 electron:
- Mỗi nguyên tử F có 8 electron (đạt octet) ✓
- Nguyên tử S có 12 electron (mở rộng octet) ✓
- Điện tích hình thức của tất cả nguyên tử = 0 ✓
Lưu ý quan trọng: SF6 là ví dụ điển hình của phân tử vi phạm quy tắc octet. Nguyên tử trung tâm (S) có 12 electron hóa trị, nhưng phân tử vẫn bền vững vì lưu huỳnh thuộc chu kỳ 3, có obitan d trống để chứa thêm electron.
Đặc Điểm Cấu Trúc và Liên Kết Trong SF6
Hình Học Phân Tử
Công thức Lewis của SF6 cho thấy phân tử có cấu trúc bát diện đều (octahedral) với:
- Góc liên kết F-S-F = 90° (giữa các vị trí kề nhau)
- Góc liên kết F-S-F = 180° (giữa các vị trí đối diện)
- Độ dài liên kết S-F: 156 pm
Phân Tích Liên Kết
Tất cả sáu liên kết S-F trong SF6 đều là:
- Liên kết σ (sigma): Hình thành từ sự xen phủ trực diện giữa obitan lai hóa sp³d² của S và obitan p của F
- Liên kết cộng hóa trị phân cực: Do độ chênh lệch độ âm điện ΔEN = 3.98 – 2.58 = 1.40
Tuy nhiên, phân tử SF6 là phân tử không phân cực do cấu trúc đối xứng hoàn toàn, các moment lưỡng cực triệt tiêu lẫn nhau.
Các Trường Hợp Đặc Biệt Khi Viết Công Thức Lewis
Phân Tử Có Số Electron Lẻ
Ví dụ: NO (nitric oxide) có tổng số electron hóa trị là 11 (lẻ), không thể tạo octet hoàn chỉnh cho cả hai nguyên tử.
Phân Tử Thiếu Electron
Ví dụ: BF3 (boron trifluoride) – nguyên tử B chỉ có 6 electron hóa trị, không đạt octet nhưng vẫn bền.
Phân Tử Mở Rộng Octet
SF6 thuộc nhóm này. Các phân tử khác: PCl5, XeF4, IF7. Điều kiện: Nguyên tử trung tâm phải thuộc chu kỳ 3 trở lên (có obitan d).
Bài Tập Vận Dụng
Câu 1: Số liên kết σ trong phân tử SF6 là bao nhiêu?
A. 5
B. 6
C. 7
D. 8
Đáp án: B
Giải thích: Mỗi liên kết S-F là một liên kết đơn, tức là một liên kết σ. SF6 có 6 liên kết S-F nên có 6 liên kết σ.
Câu 2: Số cặp electron tự do trên nguyên tử lưu huỳnh trong SF6 là:
A. 0
B. 1
C. 2
D. 3
Đáp án: A
Giải thích: Nguyên tử S sử dụng hết 6 electron hóa trị để tạo 6 liên kết với F, không còn cặp electron tự do.
So Sánh SF6 Với Các Hợp Chất Tương Tự
| Hợp chất | Số liên kết | Cấu trúc | Mở rộng octet |
|---|---|---|---|
| SF2 | 2 | Góc | Không |
| SF4 | 4 | Bập bênh | Có (10e) |
| SF6 | 6 | Bát diện | Có (12e) |
| SCl2 | 2 | Góc | Không |
SF6 là hợp chất bền nhất trong số các fluoride của lưu huỳnh do cấu trúc đối xứng và năng lượng liên kết S-F cao (327 kJ/mol).
Ứng Dụng Thực Tế của SF6
Hiểu rõ công thức Lewis của SF6 giúp giải thích các tính chất và ứng dụng:
- Công nghiệp điện: Chất cách điện trong máy cắt điện áp cao (do tính trơ và khả năng dập hồ quang tốt)
- Y tế: Chất tương phản trong siêu âm mắt
- Công nghiệp bán dẫn: Khí khắc plasma trong sản xuất chip
Tính trơ hóa học của SF6 xuất phát từ cấu trúc bền vững với sáu liên kết S-F bao quanh hoàn toàn nguyên tử lưu huỳnh trung tâm.
Nắm vững cách viết công thức Lewis của SF6 không chỉ giúp bạn giải quyết bài tập hóa học mà còn hiểu sâu về cấu trúc phân tử và liên kết hóa học. Hãy thực hành thường xuyên với các phân tử khác để củng cố kỹ năng này.
Ngày cập nhật mới nhất 09/03/2026 by Chef Kim
Chef Kim là người phụ trách phát triển hương vị và nội dung ẩm thực tại Korea House – Delivery Korea Food. Với kinh nghiệm trực tiếp trong bếp và sự am hiểu các món ăn Hàn Quốc quen thuộc, Chef Kim tập trung chia sẻ cách chế biến đơn giản, nguyên liệu dễ tìm và hương vị phù hợp khẩu vị người Việt, dựa trên quá trình nấu thử và phản hồi thực tế từ khách hàng.
